Des scientifiques indépendants demandent l'interdiction des aliments destinés aux animaux et aux êtres humains, et que, dans le même temps, toutes les plantes cultivées génétiquement modifiées soient soumises à des expérimentations.
Ce mémorandum et le rapport qui suit ont été envoyés aux personnels chargés de la réglementation [des Organismes Génétiquement Modifiés = OGM ] au Royaume-Uni et dans divers autres pays au nom de l' ISP, International Science Panel ou Jury pour une Science Indépendante. Ces informations doivent être distribuées à tous les responsables de la réglementation, aux personnels politiques et à la presse.
Source : Dr. Mae-Wan Ho , membre de l' ISP et Directrice de l' ISIS Institute of Science in Society ou Institut pour la Science dans la Société ( www.i-sis.org.uk )
Destinataires : voir la liste à la fin de ce document
Je vous écris au nom de l'ISP * Independent Science Panel pour attirer votre attention sur de récents résultats de recherche qui concernent la sûreté ou l' innocuité de protéines transgéniques et qui doivent être abordées de toute urgence.
Plus précisément, des évaluations immunologiques ont été réalisées pour la première fois avec une protéine transgénique : elles révèlent que des transformations ' post-translationnelles ' , consécutives à un transfert de gène dans une plante étrangère, ont entraîné le passage d'une protéine, jusque là inoffensive, en une protéine fortement immunogène . De plus, la protéine transgénique a entraîné des réactions immunitaires avec de nombreuses autres protéines dans le régime alimentaire. Ces résultats détaillés sont passés en revue dans le rapport ci-dessous.
Comme pratiquement toutes les protéines transgéniques impliquent un transfert de gène à partir d'autres espèces, elles sont sujettes à des transformations ' post-translationnelles ' et elles ont, de ce fait, la possibilité de devenir immunogènes . Et pourtant, aucune des protéines transgéniques qui ont été autorisées commercialement, n'ont fait l'objet d'expérimentations. Cette omission constitue un danger majeur pour la santé publique.
Nous vous invitons à imposer une interdiction immédiate à tous les aliments génétiquement modifiés et destinés à la nourriture des êtres humains et des animaux d'élevage, jusqu'à ce qu'une évaluation appropriée, sur l'immunogénicité de toutes les protéines transgéniques, ait été effectuée.
* L 'ISP a été mis sur pied le 10 mai 2003 lors d'une conférence publique à Londres. Il comprend des dizaines d'éminents scientifiques de 11 pays différents et qui couvrent de nombreuses disciplines : agronomie, agroécologie, biochimie nutritionnelle, biomathématiques, botanique, médecine chimique, écologie générale, écologie microbienne, épidémiologie, génétique moléculaire, histopathologie, physiologie, toxicologie et virologie. ( https://www.i-sis.org.uk/isp/ISPMembers.php )
Selon le Dr. Mae-Wan Ho, il faut aborder sérieusement le problème et les inquiétudes relatives à la sûreté et à l' innocuité des protéines transgéniques en général, et, dans le même temps, il faut que soit imposée une interdiction de tous les aliments génétiquement modifiés destinés aux êtres humains et aux animaux d'élevage.
Un programme conduit pendant dix ans à la Commonwealth Scientific and Industrial Research Organization CSIRO , l'organisation de la recherche industrielle scientifique du Commonwealth à Canberra en Australie, a mordu la poussière lorsque des pois génétiquement modifiés pour résister à des insectes ont causé une inflammation des poumons chez des souris [ 1 ]. Les pois génétiquement modifiés seront détruits, a annoncé le régulateur de la technologie génétique [dans ce pays], Sue Meeks.
Le gène codant pour une protéine, l' alpha-amylase inhibitor-1 (aA1) chez le haricot commun ( Phaseolus vulgaris L. cultivar Tendergreen) a été inséré dans le pois ( Pisum sativum L.) pour rendre les pois résistants à l'attaque des charançons des graines.
Le D r. T.J. Higgins, directeur adjoint de la division des plantes industrielles de la CSIRO et co-auteur de la publication scientifique rapportant ces résultats, a fait remarquer que c'était seulement la deuxième fois dans le monde qu'un programme de transgènèse végétale, consistant à transférer un gène d'une espèce à une autre, a été abandonné, et que cela démontrait l'efficacité de la réglementation stricte concernant la recherche sur les plantes cultivées génétiquement modifiées.
Le m ilitant de Greenpeace, Jeremy Tager, a précisé que cela montre tout simplement l'échec de la science par rapport à ce produit génétiquement modidié.
Le directeur du réseau GeneEthics , Bob Phelps, a considéré ce programme comme ' un gaspillage de l'argent public ' et il a souligné l'inquiétude croissante, à travers le monde, concernant les impacts des aliments génétiquement modifiés sur notre santé.
Il y a en effet d'importantes leçons à tirer de ces résultats scientifiques [ 2 ], qui soulèvent de sérieux problèmes de sécurité ou d' innocuité des protéines transgéniques en général.
Les chercheurs ont constaté que la protéine transgénique avait été transformée de manière différente [par rapport à la protéine originale] et qu'elle avait provoqué des réactions immunitaires qui ne se produisaient pas avec la protéine d'origine (voir plus loin).
La protéine transgénique aA1 [du pois] a été comparée à la protéine non transgénique [du haricot] par Western blot , une technique qui sépare les différentes formes d'une protéine qui apparaissent avec l'alpha-amylase inhibitor-1 (aA1). Des études antérieures avaient montré que la protéine indigène dans le haricot est scindée en deux chaînes, a et ß, qui ont toutes deux subi une glycolisation (par adjonction de chaînes glucidiques supplémentaires), avec un ou plusieurs acides aminés qui sont supprimés à l'extrémité de la chaîne.
Il en résulte des formes principales de chaînes a et ß ayant des masses moléculaires de 11.646 Da et 17.319 Da respectivement, ainsi que des formes mineures contenant des chaînes glucidiques alternatives.
Le transgène chez le pois a produit des chaînes a et ß avec les masses moléculaires autour de 11.000 et 18.000 Da , mais avec un modèle de bandes différentes par rapport à la protéine indigène d'origine.
Des comparaisons plus détaillées effectuées par spectroscopie de masse ont prouvé que la chaîne transgénique a était moins fortement glycosylée; par ailleurs une forme avec deux résidus de mannose en moins (de masse moléculaire de 11.322 Da ) était dominante chez le pois transgénique, mais moins abondante que chez le haricot. La chaîne ß de la protéine transgénique [chez le pois] a également montré un certain nombre d'autres bandes à côté des formes principales et mineures qui existent dans la protéine indigène d'origine [chez le haricot].
Des souris ont été nourries avec environ 25mg d'une farine de graines en suspension provenant [selon les traitements expérimentaux] (a) du pois transgénique, (b) du pois non transgénique et (c) du haricot, à raison de deux fois par semaine pendant quatre semaines.
Au bout de sept jours après la fin de cette nourriture, on a injecté aux souris expérimentales, par voie sous-cutanée dans la patte, des antigènes purifiés des protéines suivantes : soit de la protéine d'origine [du haricot], soit de la protéine transgénique aA1 [du pois génétiquement modifié] ; puis le gonflement induit dans la patte a été évalué 24 heures plus tard.
Dans une deuxième expérience, les souris ont été alimentées avec des suspensions de farine de graines comme dans la précédente expérience ; puis au bout de sept et neuf jours après la fin de ce régime alimentaire, de l'alpha-amylase inhibitor-1 (aA1) transgénique purifié, d'un côté, et une solution tampon salée, d'un autre côté, ont été administrées dans la trachée [des souris expérimentales]. La réponse inflammatoire a été observée dans leurs poumons 24 heures plus tard.
Les résultats ont montré que les souris alimentées avec du pois non transgénique [b] ou avec du haricot [c] , n'ont montré aucune réponse inflammatoire dans la patte ni dans les poumons, ce qui indique une réponse immunitaire normale vis-à-vis de la nourriture commune.
Par contre, les souris alimentées avec le pois transgénique [a] ont montré des anticorps IgG spécifiques au bout de deux semaines, et qui ont continué à augmenter jusqu'à la quatrième semaine. Il y avait un gonflement significatif de la patte ou une réponse hypersensible retardée , quand l'alpha-amylase inhibitor-1 (aA1) purifiée était injectée. De la même manière, l'introduction des antigènes dans la trachée a donné une réponse inflammatoire au niveau des poumons.
Afin de vérifier l'effet général de la modification génétique , l'expérience visant à vérifier cette réaction au niveau de la patte [des souris expérimentales] a été répétée avec le matériel provenant de deux autres plantes génétiquement modifiées : le lupin exprimant l'albumine des graines du tournesol ( sunflower seed albumin ou SSA en anglais) et les pois chiches exprimant l'alpha-amylase inhibitor-1 (aA1).
Contrairement à ce qui s'est produit avec le pois transgénique, les souris qui avaient été alimentées avec le lupin transgénique ou avec le pois chiche transgénique n'ont pas donné de réponse hypersensible retardée. Ceci prouve que la réponse vis-à-vis du pois transgénique était bien spécifique.
Les nodules lymphatiques péribronchiques [dans les poumons] des souris ont été examinés pour leur réponse à l'alpha-amylase inhibitor-1 (aA1) transgénique. Seuls les nodules lymphatiques des souris qui avaient été alimentées avec les pois transgéniques (a) ont répondu en produisant les cytokines d'inflammation (des facteurs cellulaire indicatifs) lorsque les souris expérimentales avaient été mises en contact avec l'alpha-amylase inhibitor-1 (aA1).
Cependant, la consommation de l'alpha-amylase inhibitor-1 (aA1) transgénique purifié, avec ou sans adjonction d' ovalbumine ont favorisé une forte réponse d'anticorps spécifiques de l'ovalbumine et elle a prédisposé les souris à l'inflammation lorsqu'elles avaient été en contact avec de l'ovalbumine dans la patte et dans la trachée.
Ceci suggère que l'alpha-amylase inhibitor-1 (aA1) transgénique avait favorisé des réactions à d'autres protéines. En confirmation de cela, les niveaux d' IgG antigène-spécifique contre d'autres protéines, telles que des globulines, la lectine et la viciline-4 du pois, ont également été sensiblement plus élevés dans le sérum des souris alimentées avec le pois transgénique que dans le sérum des souris qui avaient reçu du pois non transgénique.
Le pois transgénique a impliqué le transfert d'un gène entre deux espèces et il est généralement admis que le transfert interspécifique est beaucoup plus sûr, en comparaison du transfert de gènes entre des individus appartenant à des genres différents – de bactéries vers des plantes – comme cela s'est passé chez les espèces de plantes alimentaires génétiquement modifiées et qui couvrent des dizaines de millions d'hectares à travers le monde.
Une protéine, qui est inoffensive chez le haricot, mais qui s'exprime chez un pois transgénique, a causé une inflammation chez les souris et les recherches [rapportées ici] ont montré que la raison la plus vraisemblable réside dans le fait que la protéine est transformée de façon différente chez le pois.
De telles transformations ' post-translationnelles ' sont bien connues pour être spécifiques d'une espèce donnée et comme les modifications génétiques impliquent presque invariablement des transferts interspécifiques, on doit s'attendre, cela va de soit, à ce que les protéines transgéniques diffèrent structurellement des protéines indigènes d'origine. Sont-elles par conséquent susceptibles de provoquer également des réactions immunitaires ?
Cela pourrait ne pas se produire dans tous les cas de figure, comme les chercheurs l'ont constaté : l'albumine transgénique de graines de tournesol, ni celle du lupin transgénique, ni l'alpha-amylase inhibitor-1 (aA1) du pois chiche transgénique, n'ont donné des résultats comme ceux qui ont été observés avec l'alpha-amylase inhibitor-1 (aA1) du pois transgénique. Mais avec quelle fréquence cela pourrait-il se produire?
Les chercheurs ont admis que « dans l'état actuel de nos connaissances, nous ne connaissons pas la fréquence d'apparition des altérations structurelles ou immunologiques chez les protéines exprimées d'origine transgénique et nous ne savons pas si cela est uniquement le cas de l'alpha-amylase inhibitor-1 (aA1) exprimée et qui est d'origine transgénique » .
En outre, une fois consommée avec d'autres protéines, la protéine transgénique du pois a favorisé le ' cross-priming ' immunologique contre ces protéines, de sorte que les souris ont développé également des réactions immunitaires spécifiques vis-à-vis de celles-ci.
En d'autres termes, la protéine transgénique peut provoquer une réponse immunitaire généralisée à de multiples protéines présentes dans le régime, que ces dernières soient transgéniques ou non.
Le précédent exemple de programme de modification génétique qui avait dû être abandonné, était le transfert génétique de l'allergène de la noix du Brésil dans le soja [3], Le cas présent concerne une protéine qui a toute l'apparence d'être inoffensive.
Jusqu'à présent, aucune autre plante cultivée génétiquement modifiée, - et particulièrement celles qui ont déjà été disséminées dans les cultures au champ -, n'a été expérimentée de cette manière .
Cela doit être réalisé maintenant. Et, dans le même temps, une interdiction doit être imposée à tous les aliments dérivés de modifications génétiques et destinés à l'alimentation des animaux et des êtres humains.
Mr. Hamdallah Zedan, Executive Secretary, Secretariat of the Convention on Biological Diversity, secretariat@biodiv.org
Cc: Mr. David Cooper, Senior Programme Officer – Interagency and Program (UK and Northern Ireland), david.cooper@biodiv.org
Mr. Geoffrey Podger, Executive Director, European Food Safety Authority Geoffrey.podger@efsa.eu.int
Cc: Mr. Herman.Koeter, Director of Science, European Food Safety Authority, Herman.koeter@efsa.eu.int
Dr. Harry Kuiper, Chair of the GMO Panel, EFSA, h.a.kuiper@rikilt.wag-ur.nl
Colin Ross, Food Standards Agency, UK, colinRoss@foodstandards.gsi.gov.uk
Cc: Elliot Morley MP, Minister for the Environment, Emorley@aol.com
Rt. Hon Michael Meacher MP, meacherm@parliament.uk
Canadian Food Inspection Agency, Plant Products Directorate, Plant Biosafety Office, pbo@inspection.gc.ca
Cc:Hon Andrew Mitchell, Minister of Agriculture and Agri-Food and Minister of State (Federal Economic Development Initiative for Northern Ontario), Mitchell.A@parl.gc.ca
Mr. Mike Johanns, Secretary of Agriculture, USDA, United States Mike.Johanns@usda.gov
Cc: Dr. Ron DeHaven, Animal and Plant Health Inspection Service Ron.DeHaven@usda.gov
Mr. Stephen L. Johnson, Environment Protection Agency, USA johnson.stephen@epa.gov
Document en provenance de l'institut I-SIS The Institute of Science in Society
De sérieuses réactions immunitaires à une protéine transgénique ont été observées au niveau des poumons chez des souris expérimentales nourries avec un pois transgénique créé pour présenter une résistance à un bruche qui ravage les gousses et les graines chez cette espèce.
Dès le 21 novembre 2005, Christophe Noisette nous informait d'une note venant d'Australie et selon laquelle un pois trangénique avait dû être abandonné en raison de problèmes de santé chez les souris soumises à une expérimentation avec de la farine des graines de cette OGM [ Document 1 ]. Le 21 novembre, Christian Berdot des 'Amis de la Terre' des Landes, nous répercutait l'information qui était également diffusée sur le réseau ATTAC le lendemain 23 novembre 2005.
En remontant au site des agriculteurs désireux de maintenir une agriculture soutenable ou durable sur leurs exploitations en Australie, [site : www.non-gm-farmers.com/index.asp ] , nous pouvons suivre la genèse de la mise à jour des effets néfastes sur la santé des souris expérimentales nourries avec un pois transgénique résistant aux bruches qui découlait d'un programme R&D conduit depuis 10 ans dans ce pays et dont l'arrêt à été prononcé. Plusieurs contributions sur ce site continuent de nous informer et d'enrichir le débat sur les risques potentiels encourus avec des OGM sur la santé des consommateurs.
Dans un communiqué de presse en date du 28 novembre 2005, notre correspondante le Dr. Mae-Wan Ho, sous les auspices de I-SIS et de ISP basés à Londres, vient de lancer une mise en garde sous forme de mémorandum à une liste de responsables de la réglementation des OGM en Europe, aux Etats Unis et au Canada. Elle fait suivre ce mémorandum d'un rapport synthétique, de nature scientifique, qui fait un point sur les enjeux sanitaires et les recommandations qui s'imposent en la matière :
' I l faut aborder sérieusement le problème et les inquiétudes relatives à la sûreté et à l' innocuité des protéines transgéniques en général, et il faut que, dans le même temps, soit imposée une interdiction de tous les aliments génétiquement modifiés destinés aux êtres humains et aux animaux d'élevage ' .
Nous faisons suivre plus loin [ Document 2 ] la traduction en français de ce dernier document intitulé ' OGM : De sérieuses réactions immunitaires à une protéine transgénique '.
Au moment où un projet de loi sur les OGM est en préparation au Parlement français, il me semble capital qu'une large diffusion soit assurée à ce genre d'informations qui reposent sur une base scientifique, et en particulier aux personnels politiques et aux experts chargés d'émettre des jugements et des recommandations sur les OGM. Il convient que toutes ces personnes soient largement averties de ces dernières informations qui doivent tous nous interpeller.
Bon courage et bien à vous.
Jacques Hallard, Ing.CNAM, consultant indépendant – Adresse : 19 Chemin du Malpas 13940 Mollégès France - Courriel : jacques.hallard@wanadoo.fr
alpha-amylase inhibitor-1 ou aA1 : substance de nature protéique qui ralentit ou empêche l'action d'une enzyme, l'amylase. Cette dernière a la propriété d'accélérer la dégradation de l'amidon et du glycogène. En particulier, les haricots contiennent cette protéine aA1 qui agit sur l'activité de l'amylase. Cette protéine aA1 est nocive pour certains ravageurs des graines du haricot.
Anticorps: toute substance étrangère fabriquée par le corps en réponse à la présence d'un agent étranger ou antigène. La fabrication de l'anticorps est l'une des manières dont le corps se défend contre un antigène spécifique.
www.smartwork.org/pubs/pdf/fr/fr-apps-8-9.pdf
Antigène : terme qui désigne une fonction (aptitude à être reconnu par le système immunitaire = 'antigénicité') et non pas seulement une structure biochimique. Il peut d'agir d'une molécule ou d'un complexe moléculaire de nature protéique : toxines, enzymes ou molécules étrangères à un organisme vivant donné. Lorsque ces substances sont introduites dans un organisme vivant ou qu'elles sont en contact avec lui, elles induisent et provoquent une réaction immunitaire, c'est à dire la formation de facteurs réactionnels appelés anticorps spécifiques. D'une manière générale, on appelle antigène toute substance étrangère à un organisme vivant et qui est capable de déclencher une réponse immunitaire visant à l'éliminer. Les antigènes servent à identifier chaque type d'envahisseur dans un organisme touché, puisque la substance en cause est toujours étrangère à ce que l'organisme connaît. Pour en savoir plus, se reporter au travail de Delphine Grézel sur le site suivant : |
' Cross-priming ' : un phénomène par lequel des structures similaires à des virus agissent comme un adjuvant en transportant des séquences peptidiques dans une cellule présentant un antigène et qui s'attaquent aux peptides dans un processus de transformation intracellulaire. Définition d'un glossaire en anglais : www.sabin.org/vaccine_science_GlossaryB_D.htm
Cytokines : divers groupes de protéines et de peptides, glycosylées ou non, solubles, libérées plus ou moins spécifiquement par certaines cellules et qui agissent comme régulateurs humoraux à des concentrations extrêmement basses. Les cytokines contrôlent, dans des conditions normales ou pathologiques, les activités fonctionnelles des cellules individuelles et des tissus. Elles sont sécrétées par les globules blancs ou lymphocytes , les monocytes et les macrophages . Elles ont un rôle de stimulation ou d'inhibition, c'est à dire de régulation des phénomènes immunitaires. Les interleukines sont l'un des types de cytokines. Les cytokines servent de messagers dans l'information cellulaire. Pour en savoir plus, consulter le site : www.pharmacorama.com/Rubriques/Output/Cytokine.php et se reporter à l'étude de J. Bienvenu accessible par le site : bioch.ap-hop-paris.fr/analyses/Bioforma/CYTOKINE.htm
Da ou Dalton : unité de masse , un prédécesseur de l' unité de masse atomique , nommée en l'honneur du travail effectué par John Dalton sur la théorie atomique . Un dalton est désormais égal à une unité de masse atomique, soit 1/12 e de la masse d'un atome de carbone 12 C, environ 1,66056×10 -27 kg. À l'origine, un dalton était défini comme égal à 1/16 e de la masse d'un atome d' oxygène , masse qui s'avéra ensuite estimée à partir d'un mélange de plusieurs isotopes . Information récupérée de : [http://fr.wikipedia.org/wiki/Dalto... ]
Glycolisation : processus d'accrochage d'une unité glucidique à des acides aminés ou à des protéines.
IgG ou Immunoglobulines : un type de protéines du sérum sanguin qui sont produites lors d'un contact prolongé avec un antigène ou lors d'un second contact de l'organisme avec l'antigène.
Immunogène : terme qui désigne un antigène qui est en plus capable d'induire une forte réponse immunitaire une fois qu'il est administré à un individu et non pas seulement d'être reconnu dans des conditions de laboratoire. Ainsi les groupes sanguins d'un individu sont des antigènes mais ils ne sont pas immunogènes pour cet individu ; heureusement, sinon ils déclencheraient une réaction immune qui aboutirait à la destruction des globules rouges ! Très généralement, les immunogènes sont des protéines : les lymphocytes T, chargés de réguler la production des anticorps, ne reconnaissent que les protéines. Pour une étude plus détaillée, on peut se reporter au site spécialisé en immunologie vétérinaire :
www.vet-lyon.fr/ens/immuno/ENV_immuno_S5/immun07.htm
Innocuité : cara ctère de ce qui n'est ni nuisible ni toxique, qui ne constitue pas un risque pour la santé. L'innocuité des aliments doit être préservée dans toute la filière agroalimentaire, jusqu'à la bouche du consommateur . Dernier manipulateur de la filière, le consommateur partage donc avec les autres maillons de la chaîne, la responsabilité de bien choisir ses aliments et d'en préserver la qualité. Les nouvelles méthodes de production de l'agriculture industrielle, les modifications génétiques , la mondialisation des sources d'approvisionnement, l'arrivée sur le marché d'une variété de plus en plus grande de produits prêts à consommer et le recours à la restauration collective à tous les âges de la vie, contribuent à ce que la sûreté et la sécurité des produits alimentaires devienne un enjeu national et international de santé publique . Information émanant du site canadien : www.innocuite.org/
Modification ou manipulation ou transformation génétique ou transgénèse : ensemble de manipulations de laboratoire qui consistent à intégrer de l'ADN recombiné d'origine(s) diverse(s) dans du matériel vivant receveur pour donner naissance à un Organisme Génétiquement Modifié ou OGM .
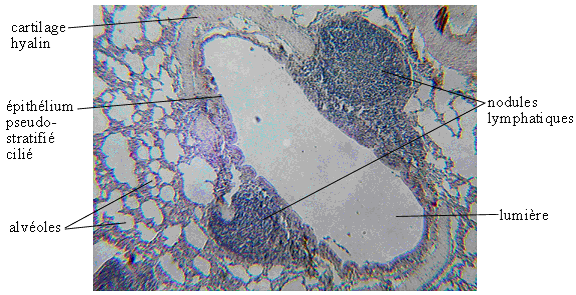
Nodules (ou nœuds) lymphatiques péribronchiques : les seuls organes lymphatiques placés sur le parcours des vaisseaux lymphatiques. Le contenu de ceux-ci, la lymphe , prend origine de l'excès de fluide intercellulaire, exsudé des capillaires veineux et recueilli par les capillaires lymphatiques. Elle se compose de lymphocytes et de fluide intercellulaire enrichi de produits de la digestion, ceux des graisses en particulier. Les capillaires lymphatiques s'unissent pour former de plus gros vaisseaux, eux-mêmes tributaires de vaisseaux encore plus gros qui rejoignent, finalement, le canal thoracique et le canal lymphatique droit. Ceux-ci se déversent dans la circulation veineuse. Les vaisseaux lymphatiques d'un certain calibre sont munis de valves qui empêchent la lymphe de circuler à rebours. Selon le site suivant : mapageweb.umontreal.ca/cabanat/bio2412/Chapitre11.html . Ces nodules drainent la lymphe de la plupart de nos tissus. Les antigènes sont filtrés dans les nodules avant de retourner en circulation dans la lymphe. Les nodules lymphatiques se retrouvent un peu partout dans l'organisme, et en particulier au niveau des poumons. Voir la photo suivante extraite du site www.callisto.si.usherb.ca:8080/ rblouin/histo/immu/nodules/nodule.htm |
|---|
Photo d'un nodule lymphatique de bronche |
 |
OGM : O rganismes G énétiquement M odifiés (on dit également transformés ou manipulés ou transgéniques ). Nom donné à un être vivant issu d'une cellule dans laquelle a été introduit un fragment d'ADN recombiné, étranger. L'individu OGM qui en résulte, possède dans toutes ses cellules l'ADN recombiné étranger introduit au départ et intégré dans son patrimoine génétique.
Ovalbumine : substance protéique visqueuse, classée plus précisément dans la catégorie des serpines. Elle est soluble dans l'eau et elle est capable de se figer par coagulation sous l'action de la chaleur, ce qui constitue une dénaturation irréversible. E lle ne possède pas de fonction connue d'inhibition d'autres protéines. L'ovalbumine possède des propriétés amphotères : elle se comporte comme un acide en milieu basique et comme une base en milieu acide.
Protéines transgéniques : molécules azotées complexes qui sont produites par un gène appelé transgène (voir ce mot) et qui a été implanté dans le matériel génétique d'un être vivant par modification génétique ou transgénèse
Transformations 'post-translationnelles' (néologisme issu de l'anglais post-translational) : changements moléculaires des protéines qui se produisent après l'étape de la traduction , c'est-à-dire de leur biosynthèse. Cette opération a lieu au niveau du ribosome qui reçoit les ARN de transfert (transporteurs des acides aminés) et l'ARN messager (qui contient l'information nécessaire à la synthèse de la protéine). La traduction est le passage d'un langage à un autre, la transposition d'un alphabet de 4 lettres (les bases A, U, G, C) dans l'ARN messager, à un alphabet de 20 lettres (les 20 acides aminés) dans les protéines. Le code génétique est la clé qui permet de passer d'un langage à l'autre. La traduction est notamment traitée sur le site fr.wikipedia.org/wiki/Traduction_(biologie) –
Les transformations 'post-translationnelles' doivent être considérées comme des étapes supplémentaires qui font partie de la biosynthèse des protéines et qui leur confèrent leurs véritables propriétés biologiques. Ces étapes peuvent comprendre : (1) des changements de covalence par des liaisons peptidiques, des terminaisons avec N et C et des résidus d'acides aminés en chaînes latérales ; (2) des changements non covalentes par repliements dans l'espace et l'adjonction de co-facteurs ; (3) des déplacements dans des compartiments cellulaires ciblés ; (4) l'implication de 'chaperons' moléculaires. Ces changements dans les molécules protéiques accroissent leur fonctionnalité, régulent leur activité, augmentent leur force mécanique et modifient leur reconnaissance moléculaire. Informations extraites du site en anglais : http://bass.bio.uci.edu/~hudel/bs99a/lecture26/
Réaction immunitaire ou allergie : c'est une réaction exagérée ou inappropriée de l'organisme au contact d'une substance étrangère. Notre système immunitaire nous permet de nous débarrasser d'agents pathogènes : virus, bactéries, champignons, cellules tumorales. L'antigène est la substance étrangère à l'organisme qui déclenche la réaction immunitaire. Si cette réaction immunitaire est exagérée ou inappropriée, l'antigène est appelé allergène. L'anticorps est la substance produite par l'organisme mis au contact de l'antigène. L'organisme a deux manières de répondre au contact d'un antigène : production d'anticorps (immunité humorale) et sensibilisation de certaines cellules (lymphocytes), on parle alors d'immunité cellulaire. Lorsque le système immunitaire réagit de manière trop importante ou inappropriée, il y a réaction allergique. Une réaction allergique ne se produit pas lors du premier contact avec la substance responsable, ce premier contact permettant à l'organisme de faire connaissance avec cette substance et de développer une immunité vis à vis d'elle. La réaction allergique se produira lors des contacts ultérieurs. Source d'information : www.lasante.be/maladies/allergie.htm
Réponse hypersensible retardée : l'hypersensibilité est exprimée, selon le « Vidal de la famille », par une r éaction cutanée (démangeaisons, boutons, gonflement) ou par un malaise général qui apparaît après un contact avec une substance quelconque, utilisation d'un médicament ou ingestion d'un aliment. Les principales formes d'allergie sont l'eczéma, l'urticaire, l'oedème de Quincke et le choc allergique (choc anaphylactique). L'allergie alimentaire peut également se traduire par des troubles digestifs. Dans le cas d'une réponse hypersensible retardée, l a réaction obtenue par l'antigène se produit relativement lentement et elle se met en place par l'intermédiaire des lymphocytes T et des macrophages. Les lymphocytes T, par les récepteurs spécifiques de leur membrane cytoplasmique, assurent la reconnaissance de l'antigène et la spécificité de la réaction. Ces lymphocytes T circulent constamment dans les tissus à partir du sang pour traverser les ganglions lymphatiques et puis rejoindre la circulation sanguine par les vaisseaux lymphatiques. Lorsqu'ils rencontrent l'antigène au niveau d'un tissu, en présence de cellules accessoires (cellules interstitielles présentant l'antigène), ils sont activés et libèrent une série de lymphokines, substances agissant sur différentes catégories de cellules. Les mécanismes divers et complexes des messages intercellulaires, qui interviennent dans les réactions d'hypersensibilité, sont notamment détaillés sur les site suivant : look4.free.fr/alergo/hs4.htm
Spectroscopie de masse : technique de chimie analytique qui utilise le principe du mouvement et de la déviation des ions dans un champ électrique ou dans un champ magnétique pour les isoler, les caractériser et de les classer en fonction de leur rapport masse/charge.
Sûreté : l a sûreté biologique concerne toutes les mesures de prévention permettant d'éviter la perte d'intégrité biologique, en particulier dans le domaine de la santé humaine et de l' écologie . Elle se rapporte entre autre à l'agriculture en référence aux risques suivants : contamination s génétiques ( virus ou gènes transgéniques ), contamination par des prions ( épizootie d' encéphalopathie spongiforme bovine ), ou à la réduction des risques de contaminations bactériennes ). Dans le domaine médical, la sûreté biologique fait par exemple référence aux transplantations d'organes ou de tissus d'origine biologique, à la thérapie génique , aux risques de maladies virales, aux maladies nocosomiales , ou aux différents niveaux de protection dans certains laboratoires. Jusqu'à présent, la sûreté biologique est essentiellement perçue comme relative au secteur agricole, mais certains groupes de pression cherchent à étendre sa définition jusqu'aux risques post-génétiques : nouvelles molécules, formes de vie artificielles, voire des robots , qui pourraient déstabiliser la chaîne alimentaire . Certains estiment que la sûreté biologique nécessite l'application du principe de précaution , et qu'une nouvelle définition axée sur la nature biologique de l'organisme menacé, plutôt que sur la nature du danger lui-même. En présence de dangers tels que les robots, la guerre biologique ou les bactéries artificielles [génétiquement recombinées], les mesures de précautions appliquées dans le cadre de la sûreté biologique ne sont probablement pas suffisantes, mais elles concernent plutôt le domaine plus complexe de la sécurité biologique . Information récupérée du http://fr.wikipedia.org/wiki/S%C3%BBret%C3%A9_biologique
Transgène : c'est une suite ou séquence de bases nucléiques, isolées d'un ou de plusieurs gènes, qui est construite et utilisée en vue de son intégration dans une cellule dans le but de modifier ou de transformer génétiquement celle-ci. Le but est de régénérer ensuite un individu fonctionnel ou OGM = O rganisme G énétiquement M odifié. Un transgène peut être conçu et réalisé à partir d'une ou de plusieurs espèces différentes.
Article first published 28/11/05
Got something to say about this page? Comment